РЕГУЛЯРНЫЕ ФАКТОРЫ НЕУВЕЛИЧЕНИЯ ЭНТРОПИИ
I. Безразмерные величины
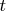
- время в единицах

- характерного времени задачи (для периодических процессов - период).
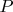
- поток тепла в единицах

- падающего на систему через поверхность

потока тепла.
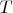
- температура в единицах

.
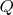
- тепловая энергия в единицах

.
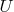
- внутренняя энергия в единицах

.
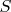
- энтропия в единицах

.

- теплоемкость при постоянном объеме в единицах

,
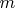
- масса нуклона.
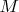
- масса нагреваемого тела в единицах

,
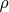
- плотность, тела,
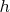
- глубина прогреваемого слоя.
Если уравнения записывать в безразмерном виде, то в них

,

,

. Эти символы сохраняются для удобства.
II. Отсутствие «откачки» энтропии «насосом» при нагреве и переизлучении в вакуум.
http://gravi.nm.ru/termodin/ris1.jpg?
Рис.1. Гетерогенная закрытая система (планета), поглощающая тепловой поток излучения (солнца), нагревающаяся и излучающая его в вакуум. Вращение, биосфера, диссипативные процессы (трения) отсутствуют.
Если допустить, что излучение тела практически чернотельное

, то система описывается уравнениями :
(1)

,
(2)

,
(3)

,
(4)

.
Интегрирование (1)-(4) дает

,

:
(5)

(6)

,
где
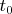
,

,

- начальные значения величин,

,

.
Качественные зависимости

,

:
http://gravi.nm.ru/termodin/ris2.jpg?
Рис.2. Зависимости а)

, б)

при поглощении излучения планетой и переизлучении его в вакуум.
Выводы :
1. При

достигается состояние термодинамического равновесия с солнечным излучением :

,

с максимальной энтропией

.
2. Температура и энтропия монотонно возрастают :

.
3. «Энтропийного насоса» (превышения экспорта энтропии над ее импортом), описываемого формулой :
(*)

, -
не существует. Производство энтропии

в такой системе всегда положительно :
(**)

.
III. Вращение как регулярный стабилизирующий фактор
http://gravi.nm.ru/termodin/ris3.jpg?
Рис.3. Температура и потоки тепла на вращающейся планете.
Пусть

- период вращения (планеты). В безразмерных единицах

. Тогда в асимптотике в системе, описанной в п.II, при

установится стационарное периодическое состояние с

, при котором энтропия (6), являясь функцией состояния, будет сохраняться :
(7)

,
где

,
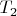
- температура, устанавливающейся на солнечной (дневной) и теневой (ночной) стороне соответственно.
Покажем, что при этом стационарные значения температур и энтропии будут меньше, чем в состоянии термодинамического равновесия со средой.
Уравнение для

:
(8)

,
где

.
Его решение на дневной и ночной сторонах

:
(9)


,
(9)


.
Если на решение (9)

наложить условия сшивки на любом
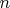
-м обороте планеты вокруг своей оси,
(10)

,
то при
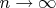
они дадут :
(11)

,

.
Подставив (11) в (9), получим соотношения на

:
(12)

.
Зависимости

и

:
http://gravi.nm.ru/termodin/ris4.jpg?
Рис.4. Зависимости

и

без вращения (1) и с учетом вращения (2).
При достижении стационарного состояния при

температура

будет периодической функцией времени :
http://gravi.nm.ru/termodin/ris5.jpg?
Рис.5. Колебания температуры на ночной и дневной сторонах вращающейся планеты.
Выводы :
1. Стационарные значения

,

меньше их максимальных значений в отсутствии вращения в равновесном состоянии

и

.
2. Регулярный неслучайный процесс – вращение – уменьшает энтропию и температуру термодинамической системы и стабилизирует ее в стационарном состоянии, далеком от термодинамического равновесия.
IV. Тепловое взаимодействие закрытых частей изолированной системы
Если закрытая подсистема только лишь излучает тепло во внешнюю среду, то, если пренебречь диссипативными процессами, её энтропия будет уменьшаться. Тем не менее, правильным с точки зрения термодинамики выводом будет такой : в неизолированной закрытой подсистеме (обменивающейся с другими подсистемами лишь потоками теплового излучения) в термодинамическом процессе между последовательными равновесными состояниями энтропия будет расти.
Рассмотрим две закрытые обменивающиеся тепловыми потоками части изолированной системы, вначале находившиеся в тепловом равновесии при температуре

. Затем в первую часть за время

инжектируется тепловой поток

при температуре

(Рис.6).
http://gravi.nm.ru/termodin/entr_umensh.JPG?
Рис. 6. Изолированная система из двух закрытых частей.
Диссипативными процессами (лишь усугубляющими ситуацию) пренебрежем. Тогда энтропию и температуру первой и второй частей системы можно найти из следующей системы уравнений :
(13)

,

где

- поток тепла в первую часть системы из второй части, измеряемый в единицах

,

- поток тепла в первую часть извне для её нагрева и выведения системы из равновесного состояния,

- единичная функция.
Численное решение системы дифференциальных уравнений (13) для функций

представлено на рис.7.
Энтропия обеих частей, как следует из уравнений (13), ввиду того, что она является функцией состояния, также будет возрастать в последовательности этих двух состояний :

,

.
Зависимость приращения энтропии первой и второй частей от времени в данном процессе представлена на Рис.8. Видно, что, несмотря на то, что после окончания нагрева энтропия первой системы в неравновесном процессе уменьшается до своего асимптотического равновесного значения, в новом равновесном состоянии энтропия будет больше, чем в первоначальном состоянии.
http://gravi.nm.ru/termodin/temp_um1.JPG?
Рис. 7. Зависимость

.
http://gravi.nm.ru/termodin/entr_um1.JPG?
Рис. 8. Зависимость

.
Уменьшение энтропии на каком-то интервале времени переходного неравновесного процесса в закрытой подсистеме возникает из-за увеличения её энтропии на предшествующем интервале времени, когда происходил её быстрый неравновесный нагрев (за время, меньшее характерного времени релаксации системы).
Аналогичный результат получается и для открытых подсистем, обменивающихся не только излучением, но и массой : в какие-то интервалы времени возможно уменьшение энтропии в подсистеме, но между равновесными состояниями (которые всегда достижимы, если нет регулярных упорядочивающих факторов) она увеличивается.
Это подтверждает, что истинной причиной увеличения порядка в любых системах является действие неслучайных регулярных факторов.
V. Реакция фотосинтеза как регулярный фактор уменьшения энтропии
Если вращение может лишь стабилизировать температуру и энтропию в стационарном состоянии периодической смены дня и ночи, далеком от термодинамического равновесия, то химическая реакция может оказаться тем упорядочивающим фактором, который приводит к уменьшению энтропии. Покажем это на примере реакции фотосинтеза в растительной биосфере планеты.
Пусть система состоит из следующих компонент (в скобках указаны номера компонент) : грунта (5), двухкомпонентной атмосферы из углекислого газа (1) и кислорода (4), воды (2) и биосферы, представленной для простоты глюкозой (3). Будем считать, что все компоненты имеют одинаковую поверхность

, а изменение их массы, а следовательно, числа частиц

определяется изменением высот компонент

, когда протекает реакция фотосинтеза (и обратная ей реакция дыхания) :

,
в которой полная масса сохраняется,

, число молекул каждой компоненты и их приращения могут быть выражены через число молекул и приращение третьей компоненты – глюкозы :
(14)

.
Здесь
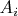
- молекулярные веса компонент в единицах

,

- стехиометрические коэффициенты, удовлетворяющие условию

;

- начальные значения числа молекул, нормированные на число

, которые можно связать с начальными плотностями компонент

и начальными высотами

участвующих в реакции и теплообмене компонент :

. Плотности компонент измеряются в единицах

, высоты компонент – в единицах длины
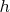
. В этих безразмерных единицах массы компонент будут измеряться в единицах

.
\
Реакция фотосинтеза протекает через множество стадий с участием большого числа ферментов. Но мы рассмотрим ее как одностадийный процесс, идущий по приведенной выше формуле, т.к., как нетрудно показать, вспомогательные компоненты не расходуются и не вносят изменений в энтропию системы.
Помимо фотосинтеза, в биосфере происходят процессы дыхания и смерти, приводящие к уменьшению массы глюкозы и кислорода и наработке воды и углекислого газа. Не будем рассматривать детальную кинетику этих процессов. Считая, что конечным результатом всех процессов будет увеличение массы глюкозы, зададим явным образом закон изменения массы глюкозы во времени, а следовательно, всех компонент системы. Скажем, линейный :

,
где

- скорость изменения высоты биосферы.
Будем также считать процесс изобарическим, пренебрежем изменением теплоемкостей в интересующем нас диапазоне изменения температуры, которую будем считать одинаковой у всех компонент.
В таких предположениях закон сохранения энергии можно записать в виде равенства скорости изменения энтальпии
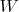
и потока тепла
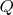
:
(15)

,
где
(16)

,

,

- удельные энтальпии компонент :
(17)

, (23)
где

- известные стандартная удельная энтальпия образования данной компоненты,

- теплоемкости при постоянном давлении. В формулах (14) – (16) энтальпия измеряется в единицах

.
Подставив (15), (16) в (14), получаем дифференциальное уравнение для нахождения зависимости температуры от времени :
(17)

Подставим в (17) выражение (14) и приведем уравнение для температуры к окончательному виду :
(18)

Здесь стандартные удельные энтальпии нормированы на

, скорость изменения высоты биосферы – на

. При учете вращения планеты характерное время задачи совпадает с периодом обращения.
Изменение энтропии в результате фотосинтеза подсчитаем в следующих предположениях. Энтропия системы равна сумме энтропий компонент,

. Энтропию данной компоненты вычислим по удельной энтропии :

. Удельная энтропия
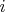
-го вещества вычисляется по формуле :

, где

– стандартная удельная энтропия
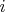
-го вещества при нормальных условиях,

К – температура при нормальных условиях, теплоемкость
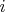
-го вещества

полагается не зависящей от температуры. Приведенная формула справедлива для случая изобарного процесса. В этой модели для изменения энтропии, нормированной на величину

, имеем следующее выражение :
(19)

.
Здесь

- начальное значение температуры. Результаты расчетов представлены на рис. 9. Зависимости температуры и энтропии от времени для планеты без биосферы в случае, когда нет вращения, и когда оно имеется были приведены ранее, на рис.4.
http://gravi.nm.ru/termodin/ris9.jpg?
Рис.9. Зависимости

и

без вращения (1) и с учетом вращения (2) на планете с биосферой.
Если рассмотреть планету с биосферой при отсутствии вращения (рис.9), то видно, что температура стремится к значению, меньшему единицы. Это значит, что реакция фотосинтеза, совершаемая биосферой, охлаждает планету, запасая энергию в образующейся глюкозе. Таким образом, достаточно мощная биосфера способна удерживать планету в состоянии, далеком от термодинамического равновесия, даже без вращения. Если же включается вращение (рис.9), то планета стремится к состоянию, еще более далекому от термодинамического равновесия.
При наличии вращения энтропия планеты с биосферой возрастает только в первые моменты времени (рис.9), пока температура возрастает. Как только температура выходит на постоянный уровень, энтропия, совершая суточные колебания, уменьшается линейно со временем. Это происходит благодаря реакции фотосинтеза, осуществляемой биосферой.
Линейный закон уменьшения энтропии в данной модели обязан лишь сделанному допущению о линейности роста массы глюкозы. Если рост массы биосферы прекращается из-за конечности ресурсов планеты, то энтропия биосферы также выйдет на стационарный уровень.
Вывод о возможности уменьшения энтропии в неизолированной системе с потоками тепла через границу под действием двух регулярных факторов : вращения и реакции фотосинтеза, - сделан в следующих упрощающих предположениях : независимость теплоемкости от температуры, постоянство давления; равенство температур реагирующих компонент; заданная постоянная скорость химической реакции вместо учета химической кинетики; применение уравнения состояния идеального газа к воде и глюкозе; упрощенное описание реакции фотосинтеза без учета её многостадийности.
Тем не менее, данные упрощения не носят принципиального характера, учет этих явлений качественно не повлияет на результат. Например, одинаковость температуры компонент обусловлена малостью скорости прироста массы биосферы по сравнению со скоростью теплообмена. Зависимость теплоемкости от температуры приводит к несущественным изменениям в приращении энтропии, т.к. вклад слагаемых с теплоемкостями компонент в (19) меньше, чем слагаемого со стандартной энтропией. Учет отличия уравнения состояния для воды и глюкозы от уравнения состояния идеального газа лишь улучшит ситуацию, т.к. энтропия жидкостей меньше энтропии газов. Детальным учетом кинетики реакции фотосинтеза можно пренебречь, т.к. нас интересует только изменение энтропии системы, а ни одно из вспомогательных веществ не расходуется и не вносит вклад в это изменение. Модель работает, когда ресурсы системы можно считать неограниченными, т.е. на начальной стадии процесса формирования биосферы.



