epros,
Цитата:
pc20b, похоже, что Вы просто не хотите ничего видеть и слышать кроме собственного мнения?
Ещё раз предлагаю Вам обратить внимание на пример с фокусировкой солнечного излучения.
1. Будете ли Вы отрицать, что тело, охлаждающееся благодаря собственному тепловому излучению, теряет энтропию?
Не будем. Это по определению

. Т.к.

,

. Но этого мало для того, чтобы делать выводы. Да, система может уменьшать свою энтропию за счет излучения энергии, но только в том случае, если предварительно она была "вброшена" на уровень с гораздо большей энтропией. При переходе же от одного равновесного состояния в другое энтропия обязательно увеличивается, если причиной этого перехода служили случайные процессы.
Цитата:
2. Будете ли Вы отрицать, что тело, нагреваемое солнечным излучением, приобретает энтропию?
Не будем в случае, если с телом не происходит никаких детерминированных процессов (например, вращение или "разумная" работа (направленная на созидание, а не на разрушение. Т.е. носящая нравственный характер). В этом случае, несмотря на нагрев солнечным излучением энтропия может и уменьшаться.
Цитата:
3. Будете ли Вы отрицать, что количество энтропии, приносимой на Землю с потоком солнечного света, не зависит от того, сфокусируем ли мы этот поток в одной области или он останется рассеянным по всей дневной поверхности?
Не будем. Это следует из закона сохранения энергии и того факта, что энтропия является функцией состояния.
Цитата:
4. Будете ли Вы отрицать, что если поток солнечного излучения сфокусирован в одной области Земли, которая в результате этого нагрета до 6000K, то некая тепловая машина может совершать работу за счёт передачи тепла от этой области в другие области Земли?
Будем. Без холодильника ЗИЛ и своевременных выплат зарплаты обслуживающему персоналу это быстро закончится.
Цитата:
5. Будете ли Вы отрицать, что температура остальной Земли при этом будет того же порядка, что и сейчас, т.е. около 300K (что она не нагреется сильнее благодаря тепловому излучению в космос и не остынет сильнее благодаря тому, что поток тепла от солнца не уменьшился)?
Будем. Если обслуживающий персонал с мехмата будет заинтересован в поддержании благоприятной экологической обстановки, то температура может и уменьшиться.
Цитата:
6. Будете ли Вы отрицать, что максимальный КПД данной тепловой машины может достигать

т.е. около 95%, а это значит, что мы сможем использовать для своих нужд до 95% от всей поступающей солнечной энергии (но не более)?
Разрешите нам над этим вопросом немного подумать.
Цитата:
7. Будете ли Вы отрицать, что биосфера могла бы в принципе тоже выступать в качестве такой тепловой машины независимо от того, что солнечное излучение рассеяно по дневной поверхности (его всегда можно сфокусировать на уровне каждого отдельного "дерева" или "листа"), и от того, вертится Земля или нет?
Не будем. Растения могут выступать в качестве машины, которая способна поддержывать планету в состоянии, далеком от термодинамического равновесия с солнечным излучением. Это удалось показать, результаты скоро будут выложены. Но деятельность растений - это детерминированный фактор.
Добавлено спустя 43 минуты 43 секунды:РЕАКЦИЯ ФОТОСИНТЕЗА КАК РЕГУЛЯРНЫЙ ФАКТОР УМЕНЬШЕНИЯ ЭНТРОПИИСуществует попытка объяснить наличие процессов, в которых происходит уменьшение энтропии, через их сопряженность с другими процессами, в которых энтропия возрастает.
В качестве примера в работе Пригожина, Дефея «Химическая термодинамика» приводится реакция синтеза мочевины из аммиака и углекислого газа, которая происходит в печени животных организмов :

В работе утверждается, что эта реакция, изменение энтропии в которой отрицательно, происходит за счет реакции дыхания (т.н. сопрягающей реакции) :

,
которая сопровождается увеличением энтропии.
Эти две реакции могут быть сопряжены следующим образом. В ходе окисления глюкозы (реакция дыхания) образуется углекислый газ, который используется при синтезе мочевины. Кроме того, для осуществления одной такой реакции необходима энергия 4-х молекул АТФ, которые также образуются в результате реакции дыхания. При разложении одной молекулы глюкозы получается 38 молекул АТФ. Если же рассчитывать на

молекулы

(стехиометрический коэффициент в уравнении реакции), то получится 6 молекул АТФ, что, как видно, больше, чем необходимо для осуществления реакции синтеза мочевины.
Рассчитаем изменения энтропии для данных реакций. В таблице приведены стандартные удельные энтропии веществ, участвующих в реакциях :
http://gravi.nm.ru/termodin/tabl_1.jpg?
Изменение энтропии в результате реакции синтеза аммиака составляет

Дж/(моль

К). Изменение энтропии в результате реакции дыхания равно

Дж/(моль

К).
Таким образом, увеличение энтропии при дыхании на порядок меньше ее уменьшения при синтезе мочевины, и суммарная энтропия системы в результате протекания двух рассматриваемых реакций уменьшается.
Следовательно, данный пример может поставить под сомнение утверждение, что энтропия может уменьшаться за счет увеличения энтропии в окружающей среде.
Итак, если вращение может лишь стабилизировать температуру и энтропию в стационарном состоянии периодической смены дня и ночи, далеком от термодинамического равновесия, то химическая реакция может оказаться тем упорядочивающим фактором, который приводит к уменьшению энтропии. Покажем это на примере реакции фотосинтеза в растительной биосфере планеты.
Пусть система состоит из следующих компонент (в скобках указаны номера компонент) : грунта (5), двухкомпонентной атмосферы из углекислого газа (1) и кислорода (4), воды (2) и биосферы, представленной для простоты глюкозой (3). Будем считать, что все компоненты имеют одинаковую поверхность

, а изменение их массы, а следовательно, числа частиц

определяется изменением высот компонент

, когда протекает реакция фотосинтеза (и обратная ей реакция дыхания) :

,
в которой полная масса сохраняется,

, число молекул каждой компоненты и их приращения могут быть выражены через число молекул и приращение третьей компоненты – глюкозы :

,


. (20)
Здесь
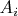
- молекулярные веса компонент в единицах

,

- стехиометрические коэффициенты, удовлетворяющие условию

;

- начальные значения числа молекул, нормированные на число

, которые можно связать с начальными плотностями компонент

и начальными высотами

участвующих в реакции и теплообмене компонент :

. Плотности компонент измеряются в единицах

, высоты компонент – в единицах длины
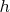
, связанной с другими нормировочными константами следующим соотношением :

. В этих безразмерных единицах массы компонент будут измеряться в единицах

.
\
Реакция фотосинтеза протекает через множество стадий с участием большого числа ферментов. Но мы рассмотрим ее как одностадийный процесс, идущий по приведенной выше формуле, т.к., как нетрудно показать, вспомогательные компоненты не расходуются и не вносят изменений в энтропию системы.
Помимо фотосинтеза, в биосфере происходят процессы дыхания и смерти, приводящие к уменьшению массы глюкозы и кислорода и наработке воды и углекислого газа. Не будем рассматривать детальную кинетику этих процессов. Считая, что конечным результатом всех процессов будет увеличение массы глюкозы, зададим явным образом закон изменения массы глюкозы во времени, а следовательно, всех компонент системы. Скажем, линейный :

,
где

- скорость изменения высоты биосферы.
Будем также считать процесс изобарическим, пренебрежем изменением теплоемкостей в интересующем нас диапазоне изменения температуры, которую будем считать одинаковой у всех компонент.
В таких предположениях закон сохранения энергии можно записать в виде равенства скорости изменения энтальпии
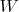
и потока тепла
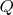
:

, (21)
где

, (22)

,

- удельные энтальпии компонент :

, (23)
где

- известные стандартная удельная энтальпия образования данной компоненты,

- теплоемкости при постоянном давлении. В формулах (21) – (23) энтальпия и количество теплоты измеряются в единицах

.
Подставив (21), (22) в (20), получаем дифференциальное уравнение для нахождения зависимости температуры от времени :

(24)
Подставим в (24) выражение (20) и приведем уравнение для температуры к окончательному виду :

(25)
Здесь стандартные удельные энтальпии нормированы на

, скорость изменения высоты биосферы – на

. При учете вращения планеты характерное время задачи совпадает с периодом обращения.
Изменение энтропии в результате фотосинтеза подсчитаем в следующих предположениях. Энтропия системы равна сумме энтропий компонент,

. Энтропию данной компоненты вычислим по удельной энтропии :

. Удельная энтропия
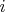
-го вещества вычисляется по формуле :

, где

– стандартная удельная энтропия
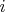
-го вещества при нормальных условиях,

К – температура при нормальных условиях, теплоемкость
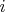
-го вещества

полагается не зависящей от температуры. Приведенная формула справедлива для случая изобарного процесса. В этой модели для изменения энтропии, нормированной на величину

, имеем следующее выражение :

.(26)
Здесь

- начальное значение температуры. Результаты расчетов представлены на рис. 12-15. На рис.12 приведены зависимости температуры от времени для планеты без биосферы в случае, когда нет вращения, и когда оно имеется. При отсутствии вращения температура стремится к единице, т.е. к температуре солнечного излучения. Таким образом, если отсутствуют и вращение, и биосфера, система приходит в состояние термодинамического равновесия с излучением.
При наличии вращения устанавливается стационарное состояние, далекое от равновесия с солнечным излучением. Температура в этом состоянии в течение суток совершает небольшие колебания вокруг значения, меньшего единицы. Таким образом, вращение обеспечивает прерывание процесса нагрева и дополнительное охлаждение планеты, что и приводит к уходу неизолированной системы от равновесного состояния с излучением.
Соответственно энтропия планеты без биосферы при отсутствии вращения (рис.13) стремится к максимуму, соответствующему термодинамическому равновесию с излучением. При наличии же вращения энтропия стремится к меньшему стационарному значению.
http://gravi.nm.ru/termodin/ris_bez_bio.jpg?
Если рассмотреть планету с биосферой при отсутствии вращения (рис.14), то видно, что температура стремится к значению, меньшему единицы. Это значит, что реакция фотосинтеза, совершаемая биосферой, охлаждает планету, запасая энергию в образующейся глюкозе. Таким образом, достаточно мощная биосфера способна удерживать планету в состоянии, далеком от термодинамического равновесия, даже без вращения. Если же включается вращение (рис.14), то планета стремится к состоянию, еще более далекому от термодинамического равновесия.
При наличии вращения энтропия планеты с биосферой возрастает только в первые моменты времени (рис.15), пока температура возрастает. Как только температура выходит на постоянный уровень, энтропия, совершая суточные колебания, уменьшается линейно со временем. Это происходит благодаря реакции фотосинтеза, осуществляемой биосферой.
http://gravi.nm.ru/termodin/ris_s_bio.jpg?
Линейный закон уменьшения энтропии в данной модели обязан лишь сделанному допущению о линейности роста массы глюкозы. Если рост массы биосферы прекращается из-за конечности ресурсов планеты, то энтропия биосферы также выйдет на стационарный уровень.
Вывод о возможности уменьшения энтропии в неизолированной системе с потоками тепла через границу под действием двух регулярных факторов : вращения и реакции фотосинтеза, - сделан в следующих упрощающих предположениях : независимость теплоемкости от температуры, постоянство давления; равенство температур реагирующих компонент; заданная постоянная скорость химической реакции вместо учета химической кинетики; применение уравнения состояния идеального газа к воде и глюкозе; упрощенное описание реакции фотосинтеза без учета её многостадийности.
Тем не менее, данные упрощения не носят принципиального характера, учет этих явлений качественно не повлияет на результат. Например, одинаковость температуры компонент обусловлена малостью скорости прироста массы биосферы по сравнению со скоростью теплообмена. Зависимость теплоемкости от температуры приводит к несущественным изменениям в приращении энтропии, т.к. вклад слагаемых с теплоемкостями компонент в (19) меньше, чем слагаемого со стандартной энтропией. Учет отличия уравнения состояния для воды и глюкозы от уравнения состояния идеального газа лишь улучшит ситуацию, т.к. энтропия жидкостей меньше энтропии газов. Детальным учетом кинетики реакции фотосинтеза можно пренебречь, т.к. нас интересует только изменение энтропии системы, а ни одно из вспомогательных веществ не расходуется и не вносит вклад в это изменение. Модель работает, когда ресурсы системы можно считать неограниченными, т.е. на начальной стадии процесса формирования биосферы.
Добавлено спустя 46 минут 32 секунды:epros,
извините, остался без ответа Ваш вопрос :
Цитата:
Я не понял, почему на "кинетической стадии" эта величина не является энтропией?
Это дело вкуса. Обычно считается, что понятие энтропии принадлежит термодинамике как модели. А она предполагает возможность усреднения микропараметров хотя бы в физически бесконечно малом объеме, чтобы существовали такие величины, как, скажем, плотность внутренней энергии, плотность энтропии и т.д. Операция усреднения - это физическая операция. Она предполагает, что между микроэлементами системы в этом малом объеме по крайней мере установились корреляционные связи (т.е. они "знают что-то друг о друге").Кинетика же - более общая модель. Она позволяет, во-первых, рассматривать систему на временах, меньших времени корреляции (или локального термодинамического равновесия), во-вторых, получать уравнения состояния.