Я думал, что, используя атомное строение вещества, а также мощный математический аппарат, физики давно вывели соответствующую теорию.
Математический аппарат страдает одной особенностью: ничтожно малую часть уравнений, которые можно с его помощью составить, можно с его же помощью решить. Просто в школе этого не видно, потому что там дают (и на математике, и на физике) только уравнения, которые известно как решать (собственно, их решению и учат). Но это капля в море.
С физикой обычно бывает так. Мягкий вариант: "Мы всё записали строго, получилось уравнение, на какой козе подъехать к его решению - у всей мировой математики no idea". Хардкорный вариант: "Бессмысленно даже пытаться записать это строго, потому что получится

уравнений, и мы не успеем их выписать прежде, чем погаснет Солнце".
Что делают физики в таком случае? Вводят упрощающие гипотезы. А давайте пренебрежём тем, тем и ещё вот этим. Вы с этим сталкивались, когда проходили идеальный газ (его, кажется, в 10-м классе проходят?). Мол, пусть у нас молекулы - это точки (что не так), и взаимодействуют они только путём соударений (что тоже не так). Зато уравнения получается такие простые, что даже Вам, школьнику, удалось понять все выкладки.
Фокус в том, чтобы найти такое упрощение (как говорят физики, приближение), чтобы и уравнения решались, и результаты с экспериментом не расходились в рамках нужной точности. Вот для воздуха в Вашей комнате теория идеального газа работает довольно хорошо. А вот для жидкости она уже совсем-совсем не работает, и процесс конденсации пара в жидкость не предсказывает.
А каково уравнение

(аналог уравнения Менделеева-Клапейрона) для жидкости? Открою Вам секрет: никто не знает. У теоретиков есть отдельные успехи для отдельных классов жидкостей (например, для жидких инертных газов). Вода в число лёгких для изучения веществ не входит: у неё водородные связи. несферические молекулы и что-то там ещё нехорошее.
У инженеров, которым некогда ждать, пока теоретики смогут, есть эмпирические уравнения, полученные из экспериментов. То есть берётся вода и измеряется толстая туча значений

, которые обобщаются в сложную формулу.Чем большей точности мы хотим добиться, тем сложнее она становится, количество коэффициентов измеряется уже десятками, и никакого понимания нам эти формулы не добавляют. Голый факт: если нагреть воду до
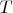
в объёме
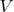
, её давление будет
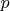
. Очень полезно, чтобы построить атомный реактор с водяным охлаждением. Совершенно бесполезно, чтобы понять что-то про устройство воды. Ну разве что очередную модель теоретиков проверять по этому уравнению, не проводя заново все эксперименты.
И кстати, полученное эмпирическое уравнение будет работать только для воды. В лучшем случае можно получить одно уравнение для класса веществ (например, жидких алканов). На жидкость в целом никто даже не замахивается.