Надо заметить, что "правильное" в этом смысле "разбиение" на макросостояния предполагает, что в равновесное состояние войдут все возможные микросостояния.
Нет, не все. Я сейчас как раз пишу (ещё не дописал) пример для температуры идеального газа, и там это очевидно.
-- 11.02.2018, 15:11 --Покажу, как получается обычная температура идеального газа по описанной выше схеме. На газ наложены макроусловия: фиксированы энергия

и пространственная область
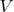
, в которой должны находиться молекулы (а полный импульс и полный момент импульса считаются, как обычно, равными нулю, и центр тяжести расположен в начале координат). Макросостояния будем характеризовать одночастичной функцией распределения

. Очевидно, что максимальное число микросостояний будет у макросостояния

, где

— равномерное распределение по области
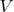
, а

— распределение Максвелла:

Энтропия такого макросостояния равна сумме вкладов

и

. Вклад

равен

, где

— объём
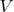
, что (поскольку число молекул
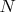
— константа, а энтропия определяется с точностью до аддитивной постоянной) эквивалентно просто

. Вклад

оказывается равен

То есть энтропия

Отсюда

и температура определяется известной формулой

Так что равновесное состояние идеального газа — это не "любое микросостояние", а только такое, при котором одночастичное распределение соответствует распределению Максвелла — Больцмана. Многие микросостояния таковыми не являются, например состояние когда все молекулы собраны в две маленьких кучки в противоположных концах сосуда, и состояние когда половина молекул движется с одной и той же скоростью влево, а другая половина — вправо.