granit201z, извините, отвечаю с запозданием (у меня быстро ответить никогда не получается).
В приведённой Вами формуле из той книги написана газовая постоянная
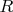
вместо постоянной Больцмана
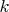
наверное потому, что автор по свойственной химикам привычке подразумевает под "энергией атома" в числителе дроби в показателе экспоненты не энергию одного атома, как было бы надо, а энергию моля вещества, вот и делит её на число атомов в моле

, так что в знаменателе дроби у него получается
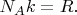
Для понимания статфизики лучше применять
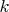
и не привязывать рассуждения к молю (понятие "моль вещества" не имеет фундаментального смысла, это просто исторически укрепившаяся в химии мера количества вещества, определённая довольно произвольным условием).
О распределении Больцмана: да, там в книге распределение Больцмана; оно менее общее, чем распределение Гиббса, оно в некотором частном случае из распределения Гиббса выводится. По форме оба распределения похожи, но по смыслу различаются. В распределении Гиббса значения

это уровни энергии изучаемой системы целиком, т.е. это уровни энергии
многочастичной системы, и, соответственно,
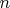
это набор квантовых чисел, которыми нумеруются квантовые состояния многочастичной системы. В распределении же Больцмана значения энергии это уровни энергии
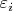
и квантовые числа
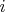 одночастичных
одночастичных состояний для частиц, составляющих достаточно разреженный газ.
О нормировке вероятности: да, Вы правильно поняли. Вот эти формулы у Вас правильные:
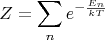
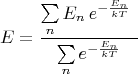
Дальнейшие рассуждения в изучении этой науки обычно развиваются по двум направлениям:
Во-первых, оказывается, можно заметить (т.е. убедиться в качестве упражнений), что если полагать, будто для конкретной изучаемой системы нам каким-то чудом удалось вычислить
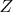
как явную функцию от

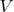
и

то для вычисления
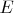
и некоторых других интересующих величин уже не надо снова заниматься суммированием (в общем случае страшно сложным) по страшно громоздким наборам квантовых чисел
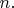
Достаточно будет просто-напросто брать производные от этой
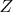
и, если потребуется, комбинировать их с самой

Например, глядя на выписанную выше формулу для

можете заметить, что
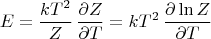
Следующий важный пример - энтропия
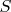
системы в состоянии теплового равновесия. Эта величина по определению выражается через усреднённый натуральный логарифм вероятности
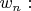
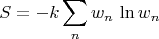
Подставив сюда формулу
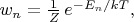
легко привести выражение для энтропии к виду
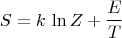
Поскольку в подобных формулах часто появляется логарифм статсуммы, то для удобства ввели для него специальное обозначение. А именно, записывают статсумму в виде
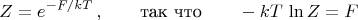
Функцию
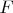
называют свободной энергией. Тогда величины

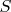
и др. можно выражать через

и притом выполняется равенство
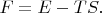
Это направление мысли удаётся обобщить дальше, если считать, что изучаемая система обменивается с термостатом не только энергией, а и частицами. Способность термостата поставлять в систему частицы заданного сорта описывается специальной величиной

называемой "химпотенциалом" частиц данного сорта. В таком варианте теории термостат описывается уже двумя переменными:
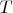
и

значения которых он "навязывает" изучаемой системе. Число частиц в изучаемой системе флуктуирует, теория позволяет вычислять усреднённое число
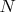
частиц в системе (оно зависит от


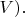
В итоге, таким путём возникает большой зоопарк формул, связывающих в общем виде разнообразные термодинамические величины.
Во-вторых (другое направление мысли), можно изучать модели систем, позволяющие писать конкретные выражения для

и с их помощью явно вычислять

А затем, разумеется, вычислять и все интересующие термодинамические величины с помощью общих формул, о которых шла речь выше.
На этом пути самый простой и в то же время важный класс моделей - так называемые идеальные газы. В основу таких моделей кладётся предположение, что в изучаемой системе энергия взаимодействия частиц друг с другом пренебрежимо мала. Тогда становится осмысленным приближённое понятие одночастичного энергетического спектра
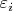
(оно будет точным, если энергия взаимодействия частиц равна нулю точно). При этом энергия системы равна просто сумме энергий отдельных частиц:
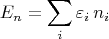
где

есть число частиц, оказавшихся в одночастичном квантовом состоянии с квантовыми числами

Многочастичное квантовое число
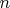
это просто совокупность значений

для всех

Если числа

могут принимать любые значения, т.е.
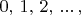
то речь идёт о так называемом бозе-газе (состоящем из бозонов). Если же числа

могут быть равными только

и

то речь о ферми-газе (состоящем из фермионов). Это, вообще говоря, квантовые газы: при достатчно низких температурах у этих газов проявляются некоторые специфические квантовые свойства.
Если для всех
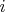
усреднённые по тепловым флуктуациям числа

(их надо как-то специально обозначать, например, как
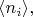
чтобы отличать от самих флуктуирующих
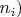
очень малы
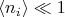
то в таком случае идеальный газ называется больцмановским. В больцмановском газе всё время большинство одночастичных квантовых состояний пустуют - они не заселены частицами. А для любого состояния, которое в процессе тепловых флуктуаций вдруг оказалось заселённым одной частицей, вероятность попадания в него ещё и второй частицы пренебрежимо мала. Т.е. в больцмановском газе числа

флуктуируют в основном между значениями

и

причём вероятность значения
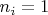
мала для каждого

А вероятностями для
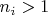
можно вообще пренебречь - они настолько маленькие, что их можно считать равными нулю. Поэтому в больцмановском случае поведение бозе- и ферми-газов становится одинаковым; их квантовая специфика не проявляется.
Результаты для термодинамических величин в больцмановском случае оказываются довольно простыми. К ним можно прийти рассуждениями из классической физики и без формализма статсуммы; подобным образом о них говорится уже в курсах общей физики, и, наверное, даже в школьных учебниках.
На этом останавливаюсь: расписывать здесь подробности не реально. И нет смысла - ведь всё есть в книгах. И коллеги здесь Вам помогут, если что-то будет совсем непонятно. А книги, конечно же, советую читать предельно внимательно и вдумчиво (не надо в книгах видеть фиги :)