В случае с колебанием все понятно - больше энергия - больше амплитуда. А с вращением? Больше энергия - больше... А что больше?
Момент импульса.
Но давайте не сразу все вопросы в одну кучу. Сначала попытаюсь ответить на этот (притом я могу внезапно "исчезнуть", не обижайтесь, - у меня из-за известных блокировок интернета возникают проблемы с загрузкой страниц этого форума):
А почему при низкой температуре в обратную сторону не происходят процессы? Т.е. вращения и колебания не возбуждаются, а, наоборот, замедляются (переходят на более низкие уровни), а поступательные движения среды соответственно ускоряются, приводя к повышению температуры?
При более низкой температуре
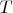
поступательные движения вовсе не ускоряются и не приводят к повышению температуры. В таких рассуждениях температура вообще считается не изменяющейся, а наперёд заданной величиной
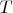
.
Рассуждаем вот как. Представляем себе, будто изучаемая система (газ, много-много атомов или молекул) помещена внутрь какой-то очень большой системы (с ещё намного большим числом частиц). Считаем, что эту большущую систему мы умеем нагреть или охладить до заданной температуры

Затем эта система "навязывает" ту же самую температуру
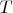
нашему изучаемому газу, который находится внутри, в полости объёмом
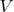
и содержит
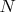
частиц (атомов или молекул заданного сорта).
Говоря другими словами (научными :), огромную систему, которая всему, что в неё засунешь, навязывает заданную температуру

называют "термостатом". А навязывание той же самой
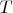
интересующему нас газу называют установлением
термодинамического или, что то же самое,
теплового равновесия между нашим газом и термостатом. Считается, что оно обязательно наступает с приемлемой точностью, рано или поздно.
Сам ход установления теплового равновесия пока не рассматриваем, а интересуемся только усреднёнными (по флуктуациям) свойствами газа уже в установившемся тепловом равновесии.
Оказывается, теоретически все такие (т.е. тепловые, термодинамические) свойства газа можно вывести из утверждения, которое выражается формулой, называемой "каноническим распределением Гиббса". Это утверждение гласит: вероятность

того, что газ находится в состоянии с квантовыми числами
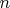
(
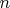
это мультииндекс, он состоит из огромного количества индексов, характеризующих квантовые состояния всех
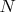
частиц газа) пропорциональна экспоненте
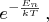
где

это энергия газа в состоянии с квантовыми числами
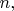
а константа

это известная постоянная Больцмана (её часто обозначают как
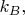
или
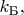
или

или вообще не пишут её, а считают для краткости записи формул, что она уже включена в определение
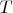
- так принято и в Ландау с Лифшицем).
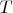
это абсолютная температура, по шкале Кельвина.
Вывод формулы Гиббса сложный; лучше его отложить на далёкое "потом". Понятие температуры
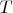
- тоже не очевидное; наверное, лучше не выяснять сразу его теоретическое происхождение, а поразбирать разные примеры применения формулы Гиббса.
При этом для понимания роли
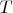
можно опираться на знания из курса общей физики и на сопутствующую физическую интуицию. Более или менее легко понимаемый интуитивно смысл
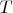
такой:

это по порядку величины энергия теплового движения частицы или какой-либо одной степени свободы в системе частиц, находящейся в тепловом равновесии с термостатом с заданной температурой

Это верно для
классических степеней свободы - таких, энергия которых не квантована или квантована с очень мелким шагом по сравнению с

так что дискретность энергетического спектра такой степени свободы не существенна, т.е. спектр энергий можно с хорошей точностью считать непрерывным.
Для существенно
квантовой степени свободы - т.е. такой, у которой интервал

между её нижним уровнем энергии и первым возбуждённым уровнем намного больше, чем

- мы, очевидно, не можем сказать, будто её энергия теплового движения порядка

Ведь такую маленькую энергию эта степень свободы не может принять или отдать. Эта степень свободы может находиться либо в состоянии на самом нижнем своём уровне энергии, либо - в возбуждённом состоянии, а оно в данном случае имеет энергию на величину
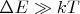
большую нижнего уровня.
Теперь посмотрите, что говорит формула Гиббса: у экспоненты в показателе знак минус, и, значит, чем больше энергия данного квантового состояния системы, тем оно менее вероятное. Например, если энергия какого-то конкретного состояния на
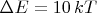
больше энергии другого состояния, то его вероятность в

раз меньше. Это и означает, что квантованные степени свободы при низких температурах (таких, что
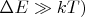
почти не возбуждаются, т.е. дают ничтожно малый вклад в усреднённую тепловую энергию системы.
Интуитивно это можно представить себе так. Разные степени свободы в ходе тепловых флуктуаций всё время обмениваются друг с другом энергией (ведь тепловое равновесие это не статическая, а динамическая картина поведения частиц в системе). Характерный масштаб энергий, которыми они обмениваются, - порядка

Но квантованная степень свободы имеет характерную дискретность энергетического спектра порядка

и поэтому может принимать и отдавать энергию только порциями порядка

Значит, при
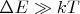
такая степень свободы долго-долго ждёт, пока другие степени свободы вдруг случайно разом передадут ей нужное количество порций

в сумме составляющие

и только тогда она переходит на свой более высокий уровень энергии. Затем она отдаст обратно эту

и опять долго-долго ждёт такой же редкой случайности. Вот и получается, что эта квантовая степень свободы чаще "сачкует" (сидит на своём нижнем уровне энергии), чем даёт вклад в тепловую энергию системы; её вклад в усреднённую тепловую энергию системы оказывается малым.
В качестве упражнения советую попробовать самостоятельно написать выражение для нормировочного множителя в указанной выше формуле Гиббса для вероятности
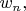
и затем выражение для усреднённой энергии
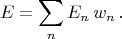
Нормировочный множитель часто обозначают как
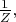
т.е. пишут:
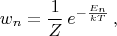
а выражение для
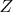
называют "статсуммой". Иногда вместо
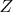
пишут
