А у инертных газов, как я понимаю, ближайшим свободным является
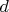
-подуровень?
Нет, у нейтральных атомов благородных газов ближайшим оказывается s-подуровень следующего уровня, как совершенно верно заметил
Mikhail_K. Однако для ионизированных атомов ситуация в некоторых случаях меняется. Например, для атома аргона достаточно однократной ионизации, чтобы 3d утонул под 4s; ксенону надо стать дикатионом, чтобы 5d стал ниже 6s; криптону же для опускания 4d под 5s надо потерять три электрона.
Я вот что лучше спрошу. В соединении

, которое только что рассматривалось, сера "не стесняется" задействовать свой 3d-подуровень. Почему же тогда аргон - "стесняется"? Да, я знаю, что инертные газы всё же иногда образуют соединения, но "очень неохотно". В чём здесь отличие от серы?
И аргон, в общем-то, не стесняется. Для него квантовохимически предсказана кинетическая устойчивость тетраоксида. По этому поводу я даже когда-то составил своим лицеистам забавную задачку:
Цитата:
Задача 1
"Папа всех бомб"
В марте 2003 года в США была создана авиабомба GBU-43/B MOAB (известная также как Mother of All Bombs) мощностью 11 тонн в тротиловом эквиваленте, что являлось на то время рекордом среди всех неядерных боеприпасов. Однако в сентябре 2007 г. Россия заявила о создании вчетверо более мощной бомбы АВБПМ, в шутку названной «Папа всех бомб». Тогда же были проведены успешные испытания этой бомбы, сюжет о которых показали по центральному телевидению. Столь большую мощность, достигаемую при массе взрывчатого заряда всего 7.1 тонн, военные объяснили применением нанотехнологий.
1. Исходя из удельной мощности тротилового заряда, равной 4.2 МДж/кг, рассчитайте удельную мощность заряда, используемого в АВБПМ.
2. Оксоанионы неметаллов 3 периода  ,
,  ,
,  ,
,  весьма стабильны несмотря на уменьшение термодинамической устойчивости высших степеней окисления в этом ряду. Например, безводная
весьма стабильны несмотря на уменьшение термодинамической устойчивости высших степеней окисления в этом ряду. Например, безводная  растворяет золото, однако её концентрированный (70%) водный раствор не восстанавливается даже двухвалентным хромом. Квантовохимические расчёты предсказывают высокую стабильность и для изоэлектронной частицы
растворяет золото, однако её концентрированный (70%) водный раствор не восстанавливается даже двухвалентным хромом. Квантовохимические расчёты предсказывают высокую стабильность и для изоэлектронной частицы  , хотя энтальпия образования из простых веществ, согласно расчётам, равна для неё 1240 кДж/моль. Предположив, что секретные нанотехнологии позволили получить оксид аргона(VIII), рассчитайте удельную мощность заряда, состоящего из смеси этого вещества с металлическим бериллием, с учётом энтальпии образования
, хотя энтальпия образования из простых веществ, согласно расчётам, равна для неё 1240 кДж/моль. Предположив, что секретные нанотехнологии позволили получить оксид аргона(VIII), рассчитайте удельную мощность заряда, состоящего из смеси этого вещества с металлическим бериллием, с учётом энтальпии образования  , равной –610 кДж/моль.
, равной –610 кДж/моль. инертные газы всё же иногда образуют соединения
За счёт пониженной энергии p-электронов по донорно-акцепторному механизму, кажись.
В дигалогенидах - да. В большинстве соединений ксенона задействованы 5d и даже слегка 4f. Для аргона удалось при низких температурах изолировать молекулу

, экзотермически выплёвывающую атом аргона с образованием фтороводорода. Для гелия предсказаны аналогичные метастабильные молекулы вроде

, а также некоторые стабильные, но малоустойчивые частицы типа

, где атом гелия образует по донорно-акцепторному механизму малопрочную связь, сравнимую по энергии с водородной. Для неона не предсказано ни одной стабильной электронейтральной частицы. (Понятное дело, в газовой фазе катионы вроде

вполне себе устойчивы.)