Нет, ну в принципе, если рассматривать ваш процесс как медленный квазистатический, то вообщем то, почти ж то в каждый момент времени мы успеваем записать

. Тогда

, что совпадает с Вашей связью если положить

. Соответственно, в любом случае работа как была

, так она и останется.

. Хотите, выражайте все через
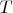
. Но там надо аккуратнее из-за квадратного уравнения относительно
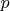
.
Вы совершенно правы, при температуре в качестве независимой переменной получается:

Возможно там где-то надо поставить дополнительные условия, или в самом интегрировании, или в упрощении

. При численной проверке все параметры сходятся до пятого значащего знака.
Правда меня покоробил сначала вид изотермической сжимаемости. В принципе одного уравнения состояния достаточно для расчета сжимаемости, термического коэффициента давления и изобарического коэффициента теплового расширения. Но это условие связи меня отвлекло и я получил не очень внятный вид для этих коэффициентов.
Тут, по моему, как раз все правильно - при независимом давлении объем находим из уравнения связи, а температуру потом из уравнения состояния.
Первая маленькая задачка, с Вашей помощью, решена, получено общее решение. Кстати, вот все частные изо-решения, когда вместо связующего уравнения записываем "параметр равен константе":



Интересно, как теперь изменится задача для Ван-дер-Ваальсова газа при теплоемкости, не зависящей от температуры и давления (потом и это учтем).



