

Опять же как то слишком просто и не участвует показатель адиабаты
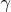
.
Знак минус не предвещает ничего хорошего, однако если предположить что такой процесс все же имеет место быть, а именно, что мы передаем газу тепло, однако его расширяют так сильно, что этого тепла не хватает чтобы компенсировать уменьшение внутренней энергрии, и температура падает. Тогда имеет место отрицательная теплоемкость, из определения

.
С другой стороны можно рассматривать определение теплоемкости как "количество тепла, необходимое чтобы
повысить температуру на 1К". Тогда нужно посчитать сколько тепла нужно для того чтобы преодолеть потери внутренней энергии из за расширения и все таки
нагреть газ.
Какое из рассуждений верно?
-- Пн май 23, 2011 20:28:21 --На мысль навела гениальность составителей задачки.
Возможно, что решение "как бы" должно выглядеть следующим образом:


тогда

и

Куда еще можно ткнуть
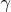
впритык не вижу.



