Всем привет
Первое начало термодинамики в математических терминах формулируется как утверждение о явном виде вариации функционала теплоты. Давайте рассмотрим частный случай, когда состояние системы определяется только давлением и температурой. Фиксируем пару каких-то состояний и будем рассматривать пути от первого ко второму.
В таком случае у нас есть функциональное пространство
![$C^{1}[T_{1}, T_{2}]$ $C^{1}[T_{1}, T_{2}]$](https://dxdy-04.korotkov.co.uk/f/7/3/b/73b7100d64fd1717eb989da6cb6df1bc82.png)
, которое содержит в себе всевозможные процессы

, удовлетворяющие нашим граничным условиям. На этом пространстве действует функционал
![$Q: C^{1}[T_{1}, T_{2}]\rightarrow \mathbb{R}$ $Q: C^{1}[T_{1}, T_{2}]\rightarrow \mathbb{R}$](https://dxdy-01.korotkov.co.uk/f/c/6/f/c6fbbe3291530cc25ddc8ba81c1dd4a282.png)
, который по процессу считает теплоту, которую к нему подвели. Автоматически считаем, что он дифференцируем по Фреше (чтобы существовала вариация и чтобы мы могли мыслить её как малое приращение теплоты при варьировании процесса).
Если у нас был какой-то процесс

из данного пространства и мы его проварьировали, то первое начало термодинамики говорит
![$Q[P(T), \delta P] = dU + \delta A$ $Q[P(T), \delta P] = dU + \delta A$](https://dxdy-01.korotkov.co.uk/f/c/e/8/ce8d991a43d5a7f81364c4009cb7a7dc82.png)
Но что такое

здесь (в каждой точке на исходном и проварьированном процессах у нас разные
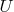
, а потому, видимо, это нельзя мыслить как приращение внутренней энергии во всех точка)? И верно ли, что

это работа на вариации?
P.S. Существуют ли изложения вариационного формализма в термодинамике на математическом уровне строгости?