Известное определение энтропии через

приводит к парадоксальному поведению энтропии идеального газа при нулевой температуре.
Это уравнение (2-е начало термодинамики) определяет энтропию с точностью до аддитивной постоянной. Проблема не во 2-м начале, а в модели классического идеального газа: она неадекватна при очень низких температурах, когда большую роль играют квантовые эффекты.
Кто-нибудь пытался переопределить энтропию?
В статистической теории энтропия интерпретируется как понятие статистики. Неформально, минус энтропия измеряет, насколько много мы знаем о системе по сравнению с ситуацией, когда все состояния равновероятны. Формально, энтропия меры
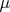
равна

, где

-- стандартная мера: в дискретном случае обычно считающая, для канонического ансамбля -- лебеговская (она же лиувиллевская)

... (В частности, для конечного множества со считающей мерой энтропия распределения вероятностей
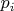
-- это минус среднее значение логарифма вероятности состояния
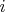
:

; слагаемые с

не учитываются.)
Нулевая температура соответствует отсутствию движения, то есть все частицы сосредоточены на поверхности

. Эта поверхность имеет нулевую меру в пространстве
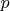
и
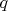
, то есть знание о том, что все частицы на ней находятся -- бесконечно подробное, поэтому и энтропия, в рамках модели классического идеального газа, бесконечна. Это противоречит 3-му началу термодинамики.