а) Если воду
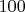
градусов закрыть в сосуде (предположим, что атмосферного давления нет), то, получается, что вода закипит?
Да, закипит, но давление быстро поднимется (если на это воды хватит конечно) и кипение прекратится (если не нагревать сосуд, ну а если нагревать, то может и сосуд разорвать ;) ).
Если вообще любую воду закрыть (с любой температурой) с учетом,
Жидкая вода не может быть быть
любой температуры. Посмотрите на диаграмму: слева -- вода замерзает, а справа -- различия между жидкой и газообразной водой пропадают.
б) Вода в открытом сосуде (с атмосферным давлением) кипит, потому что роль насыщенных паров здесь играет атмосфера как бы, которая имеет такое же давление, как давление насыщенных паров при
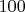
градусах,
Ну наверное можно сказать и так, но да, ровно при 100 градусах температуры по Цельсию, давление насыщенного пара воды точно равно нормальному атмосферному давлению -- это, можно сказать, определение того, что такое 100 градусов температуры по Цельсию. То есть если у вас есть закрытый сосуд, в нём налита вода и больше ничего нет (воздуха), а температура воды и сосуда составляет ровно 100 градусов по Цельсию, то можно сказать, что давление в таком сосуде равно нормальному атмосферному.