Решаю задачи
отсюда 20 и 22. У этих задач есть нечто общее, из-за чего я и испытываю когнитивный диссонанс. Это нечто заключается в следующем:
Мы видим, что оба графика состоят из двух кусков прямых, которые проходят через начало координат и некоторой кривой. Прямые соответствуют тем процессам, когда количество вещества не меняется в той части, где вода, а кривая соответствует тому процессу, когда вода испаряется и количество пара увеличивается. Так вот, из графика к задаче 20 следует, что вода начинает плавится при достижении
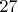
градусов Цельсия (

Кельвинах) и кипит при
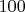
градусах Цельсия. Неужели если внешнее давление увеличить по сравнению с атмосферным в
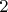
раза, то температура плавления так резко изменится? И почему давление насыщенных паров при температуре
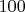
градусов равно двойному атмосферному, а не просто атмосферному?
В задаче 22 же получается, что до достижения температуры в
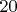
градусов азот сдавливает воду, потом, при достижении этой температуры, она начинает резко испаряться, а при достижении температуры

градусов она испаряться прекращает. Понять, почему при достижении

градусов вода перестает испаряться, можно - просто вся вода закончилась. Но почему она начинает испаряться именно при
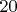
градусах Цельсия - непонятно.