Задача писал(а):
При адиабатическом расширении кислорода (

= 2 моль), находящегося при нормальных условиях, его объем увеличился в 3 раза. Определить изменение внутренней энергии газа. Ответ: –4,03 кДж
Получил такое выражение:

. Всё хорошо, но откуда мне брать

? Вроде никаких соотношений для него нету больше, чтоб использовать тут...

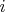
собираюсь найти, подставляя ответ. А то в разных задачах используют разные, ничего не сообщая. Иногда не соответствующие температурам.
P.S. Забыл и не могу найти нормальную температуру. Это 273 К или 293 К? Кажется, вторая.