Если считать, что скорость реакций с участием дейтерия не замедляется, как в реале (реакция

с

медленнее реакции
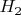
с

в 5-10 раз, по данным Химической Энциклопедии), но реакции вовсе прекращаются, то, вспоминая, что доля дейтерия

, и даже закладываясь на то, что "тяжёлая вода" принимается не дейтериевая, а дейтериево-протиевая, то есть доля её

, получим, что замена всего дейтерия на протий эквивалентна увеличению содержания воды в организме на 0.03%
А так как в норме это содержание меняется в течение дня на величины порядка процентов, то ожидать эффекта от замены воды на "лёгкую" несколько необосновано.
Что до предложения добывать "лёгкую воду" из отходов производства дейтерия, то таковых отходов, в которых доля протия выше природной воды, попросту нет.
Обычно в качестве сырья для получения дейтерия используют воду из электролизёров, в которых добывали водород (для тонкого химсинтеза; массово водород получают из природного газа). В ней содержание дейтерия вырастает до 0.1%-0.2%, затем изотопным обменом с сероводородом, затем электролизом щёлочи.