Помогите плз найти ошибку. Задачки очень простые, но с ответом не сходятся, скорее всего опечатки, но не факт, вобщем вот:

- расчитать стандартный тепловой эффект реакции при 298К.

:

кДж/моль

:

кДж/моль
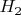
:

кДж/моль
Стандартный тепловой эффект должен быть

кДж/моль однако в ответе -168,47 кДж/моль
ещё одна:

- установите возможность (или невозможность) самопроизвольного протекания реакции при 298К.

:

кДж/моль

:

кДж/моль

:

кДж/моль
Стандартный тепловой эффект:

кДж/моль
Изменения энтропии:

:

кДж/моль*К

:

кДж/моль*К

:

кДж/моль*К
т.е в ходе реакции её изменение:

кДж/моль*К
В итоге энергия Гиббса химимческой реакции (а может и Гельмгольца, т.к. похоже что и эта и прошлая реакция идут при V,T=const, но различий всё равно быть не должно):

значит реакция не идёт, в ответе идёт.