Хет ЗифВы немножко неправильно написали равенство теплота с мат. точки зрения не является полным дифференциалом, поэтому знак дифференциала нельзя употреблять, нужно иметь ввиду что
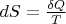
, где есть различия в обозначении малых величин, т.к. Q функция процесса, а не состояния.
-- Пт авг 21, 2009 12:26:08 --Как я понял под "кусочно-изотермическим"

имеется ввиду процесс, отдельные малые части которого можно приближенно считать изотермическими.
И, кстати, автору темы очень полезно почитать о статистическом смысле энтропии, должно все сразу стать понятно, у Матвеева, по-моему, очень хорошо написано.