Получается, что в эндотермической реакции вещества, вступающие в реакцию, сами у себя отбирают (поглощают) теплоту и охлаждают сами себя, а в эндотермической реакции сами по себе выделяют тепло и нагревают себя?.. Так сказать количество теплоты в данном случае выделяется не из-за разницы каких-либо температур, а само по себе.
Грубо говоря, да.
На молекулярном уровне, сталкиваются молекулы, реагируют, и получаются другие молекулы. У сталкивающихся молекул была какая-то кинетическая энергия. При реакции эта энергия поглотилась или увеличилась, в зависимости от конкретной реакции. И остаток раздался тем молекулам, которые получились.
У исходных молекул кинетическая энергия была в среднем равна
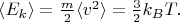
(Разумеется, сталкиваются и молекулы с большими энергиями, и с меньшими - всякие. Не всегда при таких столкновениях происходит реакция.) А у новых молекул в итоге будет какая-то кинетическая энергия, в среднем отличающаяся от величины
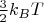
в большую или в меньшую сторону. "Растворяясь" дальше в общем тепловом движении, они либо повышают, либо понижают общую температуру смеси.
Мне кажется лучше понимать немного по-другому. Продукты реакции оказываются нагреты\охлаждены по сравнению с реагентами.
Вот это как раз неверно. Они имеют большую или меньшую энергию, но до того, как включаются в общее тепловое движение, и к ним вообще можно применять понятие температуры. Когда они включаются в общее тепловое движение, то имеют ту же температуру, что и всё остальное вещество, но эта общая температура в итоге повышается или понижается (если не добавляется потока тепла извне).
Теплота/тепловая энергия - не эквивалентное понятие термину "количество теплоты".
Это какое-то странное заявление. Боюсь, вас ТС сбил с толку, и пытаясь наводить порядок, вы навели его не в том месте.
Вообще говоря, это не обязательно будет тепловая энергия, но когда речь идет о тепловой энергии (а это, думаю, подавляющее большинство реакций)
Для полноты надо упомянуть реакции, поглощающие и выделяющие энергию в виде света.
-- 19.04.2019 16:58:57 --Я вас понял:
1) В ходе экзотермической реакции выделяется, как раз таки здесь речь об "отдать", в первую очередь отдают они себе же, а теплообмен/не теплообмен это уже дело второе (можно и без теплообмена обойтись, это не важно).
2) В ходе эндотермической реакции нужно откуда-то получать энергию и если нужно получить тепловую энергию откуда-то, то наверняка нужно создать разницу температур, чтобы ее подвести к данной реакции.
1-й пункт ещё туда-сюда (если понимать под "они" молекулы), а 2-й пункт совершенно нелепый. Никакой разницы создавать не надо. Достаточно просто нагреть реагенты.