В чём подвох?
Напомню себе. Если потенциал Гиббса задан как функция своих аргументов (
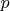
,
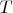
,

) то

. Следовательно,

.
Аргументы
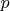
и
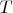
потенциала Гиббса
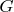
являются интенсивными величинами. Потенциал Гиббса является однородной функцией первой степени относительно (экстенсивных) переменных, задающих число частиц системы,

:
Следовательно (по теореме Эйлера об однородных функциях)
В частности, для системы состоящей из частиц одного сорта

, где
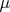
— химический потенциал этих частиц,
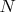
— число частиц. Т.е. если независимые переменные —
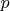
,
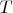
,
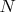
, то химический потенциал является потенциалом Гиббса на одну частицу.